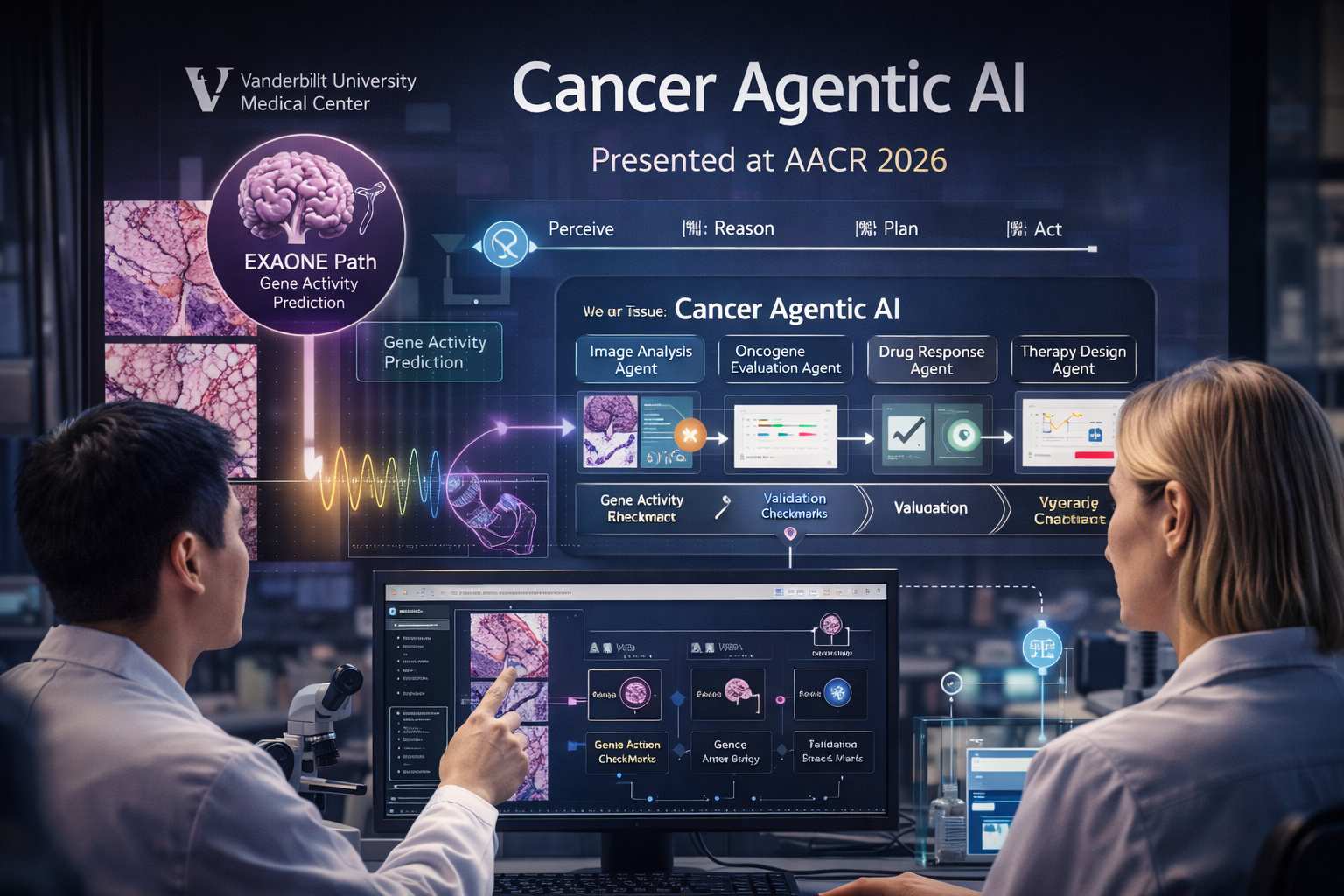
La presentazione della ricerca su “Cancer Agentic AI” da parte di LG AI Research Institute in collaborazione con il Vanderbilt University Medical Center, nell’ambito dell’American Association for Cancer Research (AACR) 2026, evidenzia un cambiamento significativo nell’applicazione dell’intelligenza artificiale in oncologia. Il progetto si colloca in una fase avanzata della transizione da sistemi AI analitici, progettati per rispondere a singole domande, a sistemi agentici complessi, capaci di orchestrare interi processi clinici in modo continuo e coordinato.
Il cuore tecnologico del sistema è rappresentato da EXAONE Path, un modello di intelligenza artificiale progettato per l’analisi patologica, in grado di inferire l’attività genica tumorale a partire da una singola immagine istologica in tempi estremamente ridotti. Questo elemento introduce un livello di astrazione particolarmente avanzato, poiché consente di derivare informazioni molecolari senza ricorrere direttamente a test genomici tradizionali, riducendo tempi e costi diagnostici. La capacità di predire l’espressione genica da dati visivi implica l’utilizzo di modelli deep learning multimodali addestrati su dataset altamente integrati, in cui immagini e dati omici sono correlati attraverso pattern complessi.
Su questa base si innesta l’architettura agentica, che rappresenta il vero elemento distintivo del sistema. Cancer Agentic AI non è un singolo modello, ma una rete di agenti specializzati che collaborano per eseguire in sequenza e in parallelo le diverse fasi del processo clinico. Ogni agente è responsabile di un compito specifico, che può includere l’analisi delle immagini, la localizzazione degli oncogeni nel tessuto, la validazione delle previsioni rispetto a dati sperimentali, la valutazione della risposta ai farmaci e la progettazione della strategia terapeutica.
Questa struttura distribuita introduce un modello operativo basato su cicli iterativi di percezione, ragionamento, pianificazione e azione. In ogni fase, l’agente elabora le informazioni disponibili, produce un output e lo trasferisce al modulo successivo, creando una pipeline decisionale continua. A differenza dei sistemi tradizionali, in cui ogni passaggio è gestito separatamente da strumenti diversi, l’approccio agentico consente una coerenza globale del processo, riducendo le discontinuità informative e migliorando la qualità complessiva delle decisioni.
Un elemento particolarmente rilevante riguarda il meccanismo di verifica interna. Il sistema è progettato per identificare autonomamente le aree di incertezza, analizzando fattori come la sicurezza delle raccomandazioni, la conformità alle linee guida cliniche, la coerenza con i dati sperimentali e la correlazione tra risposta ai farmaci e caratteristiche del paziente. Questo introduce un livello di meta-ragionamento, in cui l’intelligenza artificiale non si limita a produrre risultati, ma valuta criticamente la propria affidabilità, segnalando eventuali criticità ai professionisti sanitari.
Il ruolo dei medici rimane centrale, ma si sposta da un’attività prevalentemente analitica a una funzione di supervisione e decisione finale. Il sistema supporta il processo decisionale attraverso quattro fasi principali che includono la verifica delle caratteristiche cliniche del paziente, la previsione dell’attività genica tumorale, la validazione delle risposte ai trattamenti e la definizione della strategia terapeutica. In questo modello, l’intelligenza artificiale agisce come un amplificatore cognitivo, capace di elaborare grandi quantità di dati e presentare opzioni strutturate, lasciando al medico la responsabilità della scelta finale.
Uno degli obiettivi più ambiziosi del progetto è la riduzione drastica del tempo necessario per passare dalla diagnosi alla definizione del trattamento. Secondo quanto dichiarato, il sistema potrebbe comprimere un processo che attualmente richiede diverse settimane in un arco temporale di circa un giorno. Questo risultato è reso possibile dalla parallelizzazione delle attività e dall’automazione delle fasi di analisi e validazione, che tradizionalmente richiedono interventi manuali e tempi di elaborazione più lunghi.
L’architettura del sistema è inoltre progettata per apprendere in modo continuo. Ogni nuovo caso clinico contribuisce ad aggiornare i modelli, migliorando progressivamente la precisione delle previsioni e la qualità delle raccomandazioni. Questo approccio introduce una dinamica evolutiva che può portare a un rapido incremento delle prestazioni, soprattutto in contesti caratterizzati da elevata variabilità biologica, come l’oncologia.