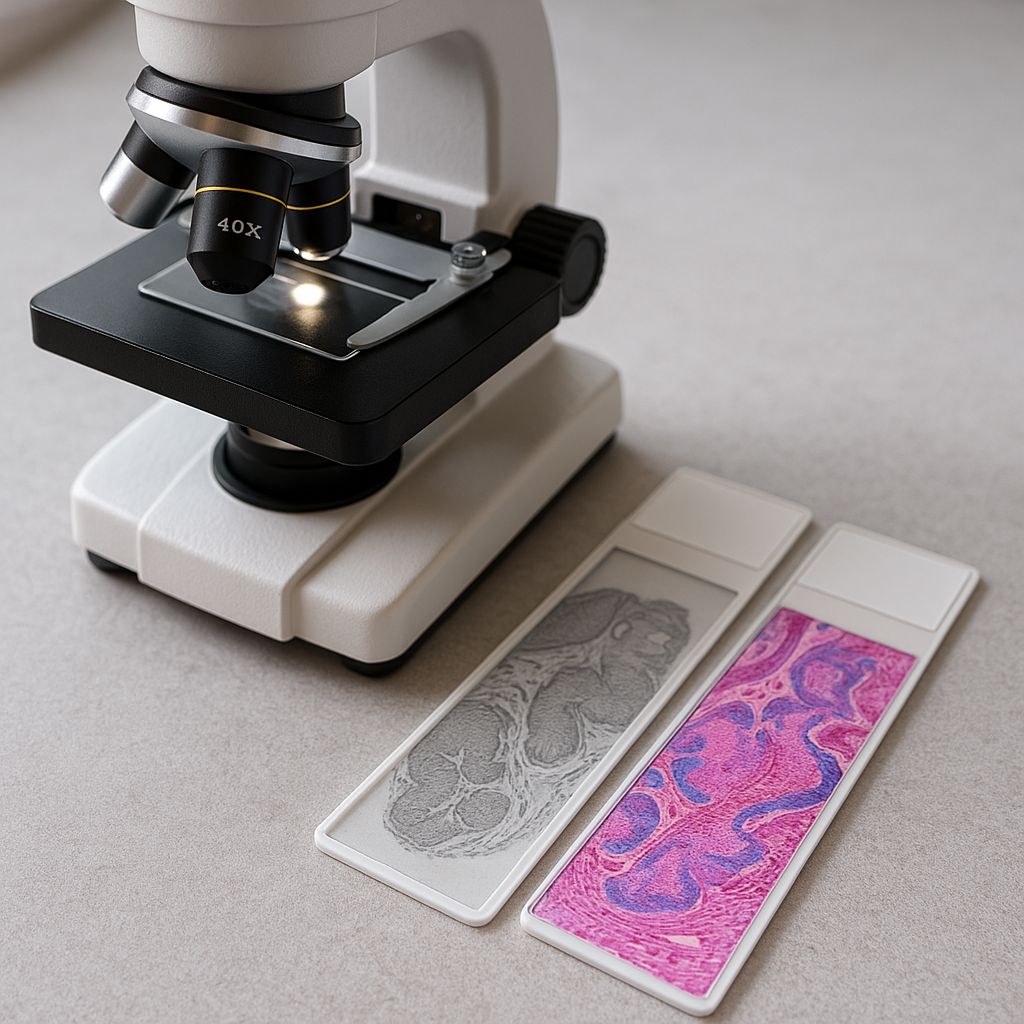
Un laboratorio patologico tradizionale si presenta con vetrini di tessuto che vengono trattati con reagenti chimici per evidenziare cellule e strutture, bagni di coloranti, tempi d’attesa, occasionali ripetizioni, sprechi e, soprattutto, il rischio di danneggiare il tessuto raro che hai a disposizione. Ora immagina di poter saltare tutti quei passaggi: carichi un’immagine “non colorata” del tessuto, l’intelligenza artificiale “dipinge” virtualmente i colori che normalmente avresti ottenuto con procedure chimiche, e tu ottieni un vetrino digitale pronto per l’analisi in pochi minuti. Questa è la promessa — già in fase di realizzazione — di Proscia, che annuncia l’integrazione di tecniche di virtual staining nella sua piattaforma Concentriq con il supporto di
La decisione di Proscia segna un punto di svolta nella diagnostica digitale: non più soltanto software per gestire vetrini digitali o applicazioni di IA su immagini colorate, ma la capacità di trasformare immagini grezze, non trattate, in versioni “colorate digitalmente” che riproducono gli effetti dei classici coloranti istologici. In pratica, portare il processo chimico-colorazione nel dominio digitale. Secondo l’annuncio, questo consentirà a un laboratorio di risparmiare tempo, eliminare reagenti chimici costosi, evitare tagli extra al tessuto (re-cuts) e accelerare il percorso dalla ricerca alla diagnosi clinica.
L’approccio si basa sulla tecnologia di Pictor Labs, che utilizza modelli di IA per generare colorazioni equivalenti ai comuni trattamenti istologici: H&E (ematossilina e eosina), IHC (immunoistochimica) e altri tipi speciali di colorazione. Il tutto a partire da immagini “label-free” di tessuto — cioè senza che il tessuto sia stato trattato chimicamente — ottenute in condizioni controllate, e trasformate in immagini “colorate digitali” che assomigliano moltissimo alle versioni chimiche. È un lavoro di elaborazione avanzata che richiede non solo modellazione visiva, ma anche conoscenza dei pattern biologici, delle texture, dei confini cellulari, dei contrasti tipici delle diverse colorazioni.
Uno dei vantaggi evidenti è la rapidità: laddove i metodi tradizionali possono richiedere ore o giorni, il sistema virtuale promette di restituire vetrini “colorati” in pochi minuti. In laboratorio, significa che una diagnosi o una valutazione molecolare non viene ritardata dalle operazioni manuali, e che il reclamo di “non sufficiente tessuto residuo” può essere mitigato, perché con una sola scansione si possono ottenere molte versioni colorate, senza dover tagliare ulteriormente il campione.
Ma non è solo una questione di velocità: la colorazione virtuale potrebbe rendere più riproducibile il processo. Le tecniche chimiche spesso introducono variabilità: tempi di immersione, concentrazioni, condizioni ambientali possono modificare l’intensità del colore, la saturazione, il contrasto. Un algoritmo ben calibrato può garantire risultati più omogenei, verosimili, comparabili tra laboratori diversi, diminuendo il margine di errore o discrepanza.
Questa scelta tecnologica non è un vezzo futuristico: Proscia lo integra nel suo ambiente già utilizzato da migliaia di patologi e scienziati nel mondo. Concentriq, la piattaforma digitale che funge da “centro operativo” per la gestione di immagini patologiche, avrà un “menu” integrato di colorazioni virtuali, disponibili on demand, direttamente nel flusso di lavoro dei professionisti. In questo modo non è necessario esportare immagini altrove o usare strumenti esterni: l’intero processo resta centralizzato, fluido e integrato.
Tuttavia, l’avanzare di questa tecnologia apre anche interrogativi importanti. Innanzitutto: quanto è affidabile la colorazione virtuale, in tutti i casi clinici complessi? Alcuni tessuti possono avere variazioni sottili, degradazioni, artefatti che sfidano il modello. In letteratura accademica si discute delle potenziali “allucinazioni” dell’IA — cioè quando l’algoritmo “inventa” dettagli che non corrispondono al reale — e della necessità di metodi automatici di controllo della qualità per verificare che il risultato virtuale sia credibile, non falsato.
Un recente studio accademico, ad esempio, ha rivolto l’attenzione esattamente a questo aspetto: propone un metodo chiamato AQuA per valutare in modo autonomo se un’immagine colorata virtualmente contiene artefatti o allucinazioni, raggiungendo elevatissime precisioni nel distinguere istanti validi da potenziali errori. Questo tipo di verifica potrebbe affiancare o “scoraggiare” l’uso indiscriminato della colorazione virtuale in ambito diagnostico, finché non vengano stabiliti standard clinici affidabili.
Un’altra difficoltà è la generalizzazione: modelli addestrati su certi tipi di tessuti, in certe condizioni, possono non adattarsi bene a tessuti con caratteristiche diverse (tumore raro, tessuti danneggiati, artefatti di preparazione). Perché la tecnica diventi uno strumento clinico robusto, dovrà affrontare una grande varietà di casi reali. In ambito virtual staining, recenti lavori propongono architetture resilienti al “misalignment” (disallineamento spaziale) tra input non trattati e riferimenti chimici, per rendere più robusta la trasformazione. Uno studio recente parla di un miglioramento significativo rispetto a modelli precedenti proprio in presenza di disallineamenti tra vetrino reale e tessuto simulato.
Infine, c’è la questione normativa e regolatoria: una colorazione virtuale, anche se convincente, dovrà essere validata, accettata dagli organismi clinici, confrontata con metodi d’oro. Le cliniche e i laboratori vorranno garanzie: “Se uso colorazione virtuale, quanto rischio che una diagnosi venga compromessa?” I protocolli clinici richiedono standard rigorosi.
L’iniziativa di Proscia con Pictor Labs è un passo audace verso una nuova generazione della patologia digitale. Non è una promessa vaga, ma un’operazione concreta che, se ben realizzata, può accelerare i tempi diagnostici, ridurre costi, preservare campioni e rendere l’intero flusso più efficiente e armonico. Ma come ogni tecnologia emergente in campo medico, il successo dipenderà dall’equilibrio tra innovazione e rigore, tra audacia e verifiche cliniche, tra il sogno dell’“immagine perfetta con un clic” e la realtà delle cellule che hanno sempre l’ultima parola.